Du code au contrôle: Le potentiel thérapeutique de l’édition épigénétique
Alors que les thérapies géniques commencent à transformer le paysage thérapeutique pour un grand nombre de maladies, une récente étude propose un nouvel outil : la thérapie épigénétique. En ciblant un petit groupe d’éditeurs épigénétiques sur un gène précis, le Dr. Cappelluti et ses collègues ont réussi à réduire l’expression du gène PCSK9 chez la souris, qui régule la production de cholestérol. Dans cet article, nous explorerons l’émergence et le fonctionnement de la thérapie épigénétique, ainsi que les avantages qu’elle offre en comparaison aux thérapies géniques classiques dans le traitement des maladies complexes.
“Wow . . . un véritable jackpot pour la thérapie génique!”
Inder M. Verma. Alors éditeur chez Molecular Therapy, August 2000.
Seulement un mois après l’annonce de la quasi-complétion du projet « Génome Humain », qui visait à cartographier l’ensemble des gènes chez l’Homme, les chercheurs se projetaient déjà dans cette mine d’information pour potentiellement soigner les maladies génétiques1. Nous avions alors une carte, mais il manquait encore les outils. Puis, 12 ans après, vint la révolution CRISPR.
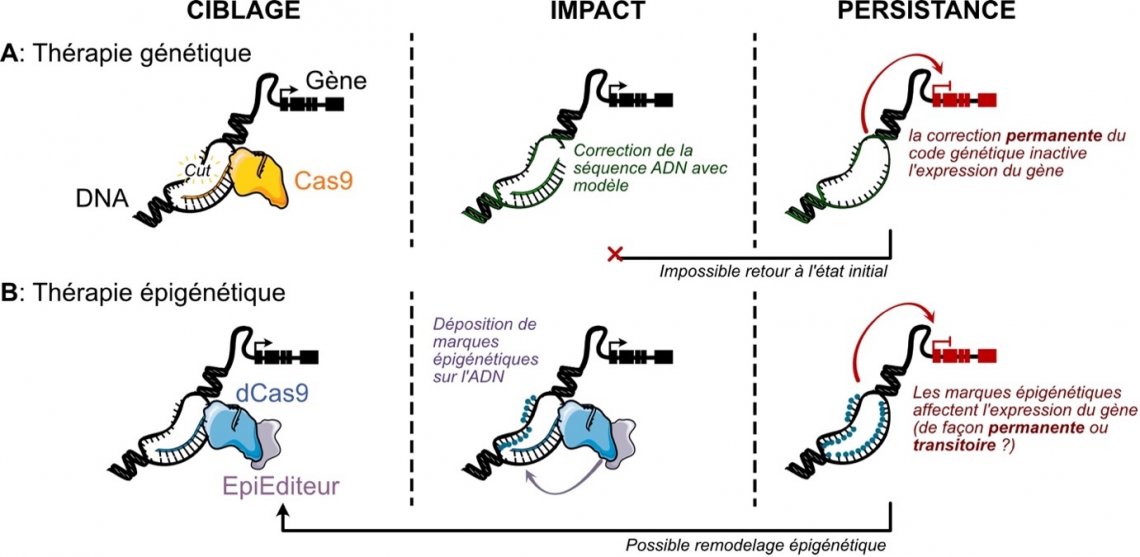
Dérivé d’un « système immunitaire bactérien », la protéine éditrice CRISPR/Cas9 (ou Cas9), fonctionne comme des ciseaux moléculaires, capables de couper précisément l’ADN en des séquences spécifiques après un ciblage précis. Cette découverte a permis aux scientifiques de supprimer et corriger des mutations de la séquence d’ADN, en apportant aux cellules mutantes un modèle correctif pour réparer leur ADN après la coupure (Figure 1A)2. Seulement un an et demi après la publication des capacités éditrices de CRISPR/Cas9, l’entreprise CRISPR Therapeutics, fondée par les auteurs de cette publication, a levé plus de 80 millions de dollars américains. Deux ans plus tard, plus de 150 brevets pour des applications utilisant CRISPR étaient déposés3. Cette course effrénée s’est conclue en 2023 avec le développement de Casvegy par CRISPR Therapeutics, the premier traitement CRISPR approuvé pour soigner les maladies du sang bien connues que sont la β-thalassémie et la drépanocytose. Ce traitement représente un bond technologique important, mais reste encore limité dans son impact. En effet le coût du traitement est estimé, au moment de l’écriture de cet article, à deux millions de dollars américains, et seulement une poignée de patients par année peuvent être traités par la compagnie4. Malgré ces défis, plus de 2000 thérapies géniques seraient en développement dans le monde, et le marché pourrait augmenter de cinq à plus de 19 millions de dollars d’ici 20275.
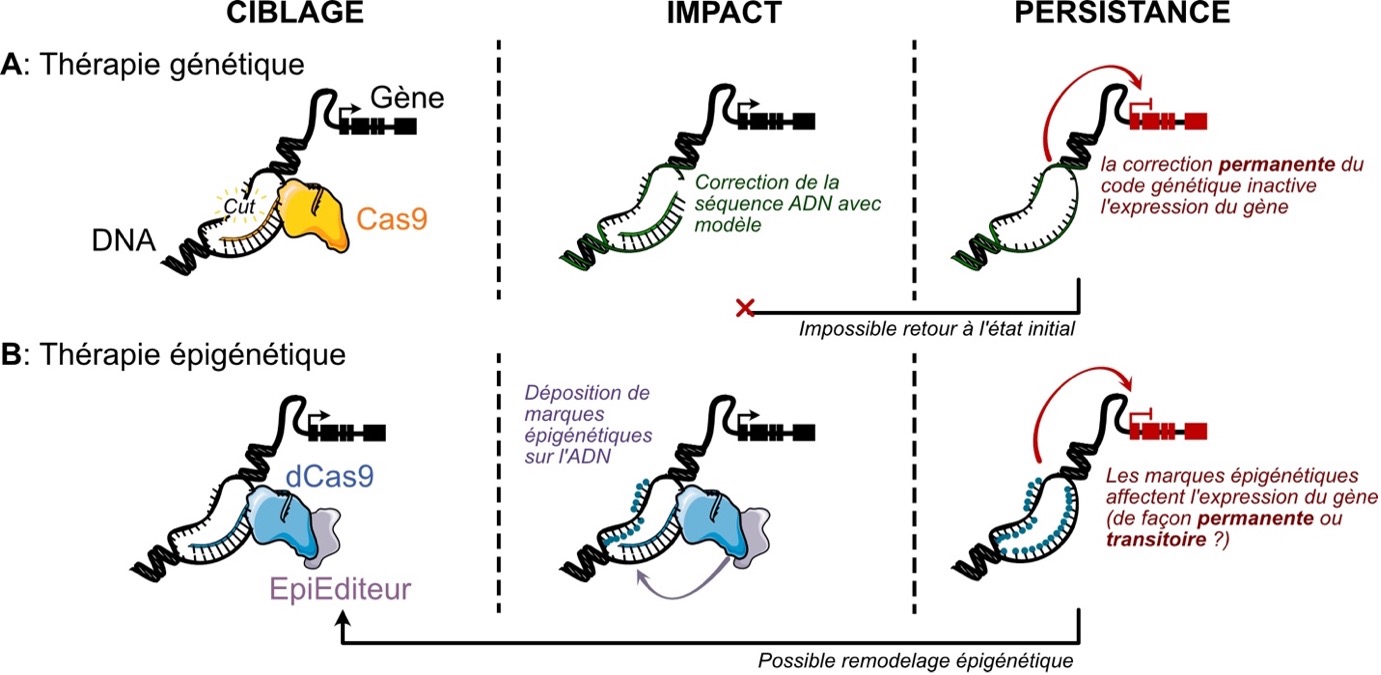
Cependant, des inquiétudes persistent concernant ces thérapies géniques. Premièrement, notre compréhension du rôle exact des gènes dans l’émergence des maladies reste limitée. Même si quelques maladies sont connues pour être directement causée par des mutations génétiques dans un seul gène, seulement 60% des malformations congénitales peuvent être associées à des facteurs spécifiques précis. De plus, des études sur jumeaux estiment que seulement 40% des maladies ont une forte composante génétique6, mais ce chiffre reste disputé et pourrait même être surévalué7. En effet, il est aujourd’hui accepté que la majorité des maladies, incluant l’obésité, le cancer, le diabète et les maladies neurologiques, sont la résultante d’un mélange complexe de facteurs polygénique (impliquant plusieurs gènes) et d’influences de l’environnement.
Une autre limitation significative de la thérapie génique est son irréversibilité. Toutes les modifications introduites par l’éditeur Cas9 sont permanentes, ce qui soulève une multitude de préoccupations éthiques et d’inquiétudes concernant de possibles effets secondaires persistants. Des erreurs de modifications génétique, ou « off-targets », en particulier, représentent un risque majeur (Figure 1A), puisque ces éditions involontaires seraient difficiles et coûteuses à identifier, les rendant difficiles à corriger. Plus simplement, si une erreur est faite, revenir en arrière serait une tâche quasi impossible.
La promesse de la thérapie épigénétique: du code au contrôle.
Les marques épigénétiques sont des modifications chimiques attachées à l’ADN et les protéines histones qui le compacte (voir notre précédent article à ce sujet : https://thisisepigenetics.ca/what-is-epigenetics). Les modifications épigénétiques peuvent promouvoir ou réprimer l’expression des gènes. Contrairement aux mutations génétiques permanentes, les modifications épigénétiques sont dynamiquement ajoutées ou retirées par des enzymes dédiées et peuvent ainsi s’adapter rapidement aux influences extérieures comme le stress, le régime alimentaire ou le vieillissement. En conséquence, les modifications épigénétiques sont centrales pour améliorer notre compréhension de l’interaction entre notre environnement et l’émergence des maladies, une complexité que la génétique pure ne parvient pas à résoudre. De fait, des médicaments épigénétique sont déjà en usage, notamment pour le traitement du cancer8. En s’appuyant sur les méthodes développées pour la thérapie génique, une étude récente publiée dans la revue Nature suggère que l’édition épigénétique peut traiter des maladies et répondre aux inquiétudes levées par l’édition génique.
Ces recherches publiées par Martino Alfredo Cappelluti and Angelo Lombardo de l’institut scientifique de San Raffaele en 2024 démontrent le potentiel de l’édition épigénétique pour réduire le « mauvais » cholestérol, LDL, chez la souris 9. Leur approche repose sur une combinaison d’éditeurs épigénétiques, en particulier ceux impliqués dans la déposition de méthylation sur l’ADN, pour réduire l’expression du gène PCSK9 dans le foie. Ce gène a été pris pour cible car il code pour une protéine qui contrôle les niveaux de LDL circulant dans le sang. Pour cibler ces éditeurs épigénétique vers ce gène dans l’ADN de la souris, les chercheurs ont testé plusieurs systèmes de ciblage, incluant une Cas9 « morte » (en anglais « dead » ou « dCas9 »), qui ne peut plus couper l’ADN, et des protéines dites « à doigts de zinc » (ou « zinc finger proteins » ZFP, en anglais) qui peuvent également se lier à l’ADN en des séquences précises (Figure 1B).
Un guide en 2 étapes pour une édition efficace du génome : « Impact et Persistance ».
Pour réaliser une édition épigénétique efficace, deux défis doivent être adressés : (i) s’assurer un impact précis (le ciblage correct et la déposition des nouvelles marques épigénétiques) et (ii) s’assurer de la persistance des modifications épigénétiques dans le temps. Ces deux éléments sont étroitement associés, car un impact fort suggère une plus grande persistance de l’effet.
Pour obtenir une réduction robuste du gène PCSK9, les chercheurs ont combiné plusieurs éditeurs épigénétiques; des ADN méthyltransférases qui modifient chimiquement l’ADN, et des histones méthyltransférases qui altèrent chimiquement les protéines histones associées à l’ADN. Leur raisonnement étant qu’une combinaison de modifications épigénétiques produirait une plus grande et longue répression du gènes PCSK9. De fait, les chercheurs ont effectivement réduit de 38-52% les niveaux d’expression de PCSK9 pendant plus de 300 jours après l’injection des modificateurs épigénétique dans le foie des souris. Cette répression de long-terme corrèle avec l’établissement d’un domaine de répression épigénétique stable proche de la cible PCSK9 avec peu de modifications indésirables9.
Globalement, ces modifications épigénétique ont réduit de 30% le cholestérol-LDL un mois après le traitement. Pour tester la durabilité de leur approche, les scientifiques ont utilisé les capacités de régénération du foie après son ablation chirurgicale (hépatectomie). En effet, même après une hépatectomie, les souris traitées ont continué de montrer une réduction de l’expression PCSK9, des niveaux de LDL sanguins, et un domaine répressif épigénétique stable pendant plus de deux mois9.
L’édition épigénétique: Une voie pour la médecine de précision.
Ces recherches font la démonstration que l’édition épigénétique constitue une voie thérapeutique viable. Ils ont pu réduire fortement et durablement le gène PCSK9, réduisant en conséquence les niveaux du mauvais cholestérol sanguin, LDL, avec peu d’effets indésirables et aucune modification du code génétique lui-même.
Cependant, des défis restent à relever. Alors que peu de modifications hors-cibles indésirables ont été détectées, quelques erreurs ont quand même eu lieu. Le système de cible dCas9 a semblé cependant montrer plus de précision que les systèmes ZFP, démontrant sa plus grande efficacité pour limiter ces effets indésirables. Enfin, la réversibilité du traitement épigénétique n’a pas été encore testée, un aspect central dans la différenciation de l’édition épigénétique par rapport à l’édition génétique permanente.
Il est aussi essentiel de rappeler les conditions expérimentales. Cette étude a été conduite chez la souris, ou tous les paramètres environnementaux (du régime alimentaire, à la température, en passant par la durée du jour) sont sous le contrôle des chercheurs. Ainsi, atteindre de tels effets thérapeutiques chez les humains, qui vivent des conditions bien plus variables reste à démontrer.
Malgré tout, les preuves sont sans équivoque: des modifications épigénétiques peuvent être introduites dans un organisme vivant, peuvent persister dans le temps et produire des effets thérapeutiques. De plus, ce nouvel outil qui étend le champ des interventions thérapeutiques possibles pour traiter des maladies complexes. En déplaçant le dogme de la modification génétique vers le contrôle épigénétique de l’expression des gènes, l’édition épigénétique promet des applications potentielles pour réduire le vieillissement et la dégénération biologique, et traiter des maladies complexes comme le cancer ou l’addiction 8,10,11.
Références.
1. Verma, I. M. & Gage, F. H. Genome and Gene Therapy. Molecular Therapy 2, 95 (2000).
2. Jinek, M. et al. A Programmable Dual-RNA–Guided DNA Endonuclease in Adaptive Bacterial Immunity. Science 337, 816–821 (2012).
3. Ledford, H. CRISPR, The Disruptor. Nature 522, 20–24 (2015).
4. Sheridan, C. The world’s first CRISPR therapy is approved: who will receive it? Nature Biotechnology 42, 3–4 (2023).
5. Bishen, S. & Doxzen, K. Why we need to accelerate global access to gene therapy. World Economic Forumhttps://www.weforum.org/stories/2022/10/gene-therapy-why-we-need-to-acc… (2022).
6. Polderman, T. J. C. et al. Meta-analysis of the heritability of human traits based on fifty years of twin studies. Nat Genet 47, 702–709 (2015).
7. Feldman, M. W. & Ramachandran, S. Missing compared to what? Revisiting heritability, genes and culture. Philosophical Transactions of the Royal Society B: Biological Sciences 373, 20170064 (2018).
8. Yoo, C. B. & Jones, P. A. Epigenetic therapy of cancer: past, present and future. Nat Rev Drug Discov 5, 37–50 (2006).
9. Cappelluti, M. A. et al. Durable and efficient gene silencing in vivo by hit-and-run epigenome editing. Nature(2024) doi:10.1038/s41586-024-07087-8.
10. Egger, G., Liang, G., Aparicio, A. & Jones, P. A. Epigenetics in human disease and prospects for epigenetic therapy. Nature 429, 457–463 (2004).
11. Janssen, S. Epigenetics and drug addiction: predisposition, chronic use, relapse and treatmentEpigenetics and drug addiction: predisposition, chronic use, relapse and treatment | This is Epigenetics. This is Epigeneticshttps://thisisepigenetics.ca/about-epigenetics/epigenetics-and-drug-add… (2023).
|
Apprendre encore plus:
|